[酸和碱的中和反应教案]《酸和碱的中和反应》教学素材(常用酸碱指示剂的变色原理)
石蕊和酚酞是常用酸碱指示剂,它们都是弱的有机酸。在溶液里,随着溶液酸碱性的变化,指示剂的分子结构发生变化而显示出不同的颜色。
石蕊能溶于水,不溶于酒精,变色范围是pH为5.0~8.0。石蕊(主要成分用HL表示)在水溶液里能发生如下电离:
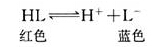
在酸性溶液里,红色的分子是存在的主要形式,溶液显红色;在碱性溶液里,上述电离平衡向右移动,蓝色的离子是存在的主要形式,溶液显蓝色;在中性溶液里,红色的分子和蓝色的酸根离子同时存在,所以溶液显紫色。
酚酞的变色范围是pH为8.0~10.O。在酸性溶液中,H+浓度较高时,它形成无色分子;随着溶液中H+浓度的减小,OH-浓度的增大,酚酞结构发生改变,并进一步电离成红色离子,如下式所示:

这个转变过程是一个可逆过程,如果溶液中H+浓度增加,上述平衡向反方向移动,酚酞又变成了无色分子。因此,酚酞在酸性溶液里呈无色,当溶液中H+浓度降低,OH-浓度升高时呈红色。
酚酞的醌式或醌式酸盐,在碱性介质中是很不稳定的,它会慢慢地转化成无色的羧酸盐式,如下式所示:

因此,做氢氧化钠溶液使酚酞显色实验时,要用氢氧化钠稀溶液,而不能用浓溶液。
来源:查字典化学网
本文来源:https://www.oubohk.cn/huaxue/359408/
酸和碱的中和反应ppt 酸和碱的中和反应教学视频




