氢氧化铁胶体的制备方程式_氢氧化铁胶体的制备


实验演示
操作方法
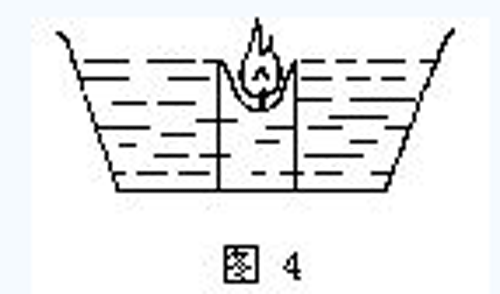
用烧杯盛20mL蒸馏水,加热至沸腾,然后滴加饱和氯化铁溶液1~2mL,继续煮沸;直至溶液变成红褐色,停止加热。
实验现象
胶体呈红褐色、透明的液体。
实验结论
FeCl3溶液属于强酸弱碱盐,在加热时促进其水解,生成胶粒分子的集合体.
实验考点
1、氢氧化铁胶体的制备方法。2、氢氧化铁胶体的颜色。
经典考题
1、用饱和的FeCl3溶液制取Fe(OH)3胶体,正确的操作是( )
A. 将FeCl3溶液滴入蒸馏水中
B. 将FeCl3溶液滴入热水中,生成棕黄色液体
C. 将FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色液体
D. 将FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色沉淀
试题难度:易
2、用下列方法来制备溶胶:①0.5mol/L BaCl2溶液与等体积的2mol/L H2SO4相混合;②把1mL饱和氯化铁逐滴加入20mL沸水中;③把1mL水玻璃溶液加入10mL 1mol/L盐酸中;④向10mL 0.01mol/L H2S溶液中逐滴加入8~10滴0.01mol/L的氯水。能够得到胶体溶液的是
A. 只有①②③ B. 只有①③
C. 只有②③④ D. ①②③④
试题难度:中
3、将铝粉逐渐投入饱和氯化铁的黄色溶液中,首先看到溶液变成红褐色,并产生气泡;后来有少量的红褐色的沉淀,并有少量的能被磁铁吸引的黑色沉淀物质生成,请回答下列问题:(1)红褐色溶液物质是_________________________,红褐色的沉淀是_____________,气泡的成分是_____________________,黑色物质是_____________________。(2)除去红褐色溶液中少量沉淀的实验方法是____________________。(3)试用简洁的文字和化学方程式解释上述实验现象:___________________________。
试题难度:难
1 答案:C
2 答案:D
解析:制取胶体的方法很多,其中用溶液制备胶体需要注意浓度一定要小。
3 答案:(1)Fe(OH)3胶体;Fe(OH)3沉淀;H2;Fe。
(2)过滤
(3)氯化铁溶液中存在着水解平衡:Fe3++3H2O 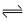 Fe(OH)3(胶体)+3H+,
Fe(OH)3(胶体)+3H+,
2Al+6H+==2Al3++3H2↑减小了c(H+),使氯化铁的水解平衡向正向移动,生成大量的氢氧化铁胶体溶液和少量氢氧化铁沉淀。Al+3Fe3+==Al3++3Fe2+,2Al(过量)+3Fe2+==2Al3++3Fe(黑色)。
解析:除了考查分析推理能力外,还考查了文字表述能力。(1)氯化铁溶液显酸性,铝粉投入饱和氯化铁溶液中可以发生置换反应产生氢气,进而又促进了铁离子水解,所以有红褐色的氢氧化铁沉淀。还有部分氢氧化铁以胶体形式存在于溶液中,所以沉淀后溶液变红褐色。
氢氧化铁胶体一定带正电吗?
在制备氢氧化铁胶体的实验中,一般为向沸水中加入FeCl3溶液,由于Fe3+的水解,使溶液显酸性,溶液中的OH-浓度较小,因此氢氧化铁胶核更容易吸附浓度较大的Fe3+,带正电,如果在碱性环境下,则可吸附OH-带负电。
由此,我们常说的氢氧化铁胶体带正电,是由于制备胶体的实验过程的特殊性决定的,而非氢氧化铁胶体一定带正电。
本文来源:https://www.oubohk.cn/huaxue/58871/
制备氢氧化铁胶体方程式 如何制备氢氧化铁胶体